وضح بالشرح الخلايا (الأعمدة) الكهربائية والبطاريات وانواعها المختلفة؟
إن الخلايا الكهربائية هي إحدى وسائل توليد التيار الكهربائي المستمر (D.C) وهذه الخلايا (البطاريات) نوعان هما:
ا - الخلايا الابتدائية Primary Cells
ب - الخلايا الثانوية Secondary Cells
ا - الخلايا الابتدائية :
هي أدوات يمكن بوساطتها تحويل الطاقة الكيميائية إلى طاقة كهربائية وتتكون من موصلين موضوعين في محلول كيميائي تأثيره في أحدهما يختلف عن الآخر مما يسبب حدوث فرق جهد بين الموصلين وهي على أنواع:
(۱) عمود فولتا. (۲) العمود الجاف. (۳) عمود لاكلانشيه.
بعد العمود الجاف أكثر هذه الأعمدة استعمالاً، ويتركب من إناء مصنوع من الخارصين يمثل القطب السالب ويحاط بعجينتين الأولى نشارة الخشب والرمل والقار لمسك عمود الكاربون في مكانه وكلوريد الخارصين وكلوريد الأمونيوم والماء من الداخل والثانية عجينة من ثنائي أوكسيد المنغنيز والكاربون وفي القلب قطب من الكاربون يمثل القطب الموجب والقوة الدافعة الكهربائية لهذا العمود (ق. د.ك = ١.٥ فولت). لاحظ الشكل رقم (2-1)

الشكل 2-1 الاعمدة الجافة
ويمتاز هذا العمود بخفة وزنه و سهولة استعماله، إلا أنه قصير الأجل لعدم سهولة تجديد أجزائه. و يستعمل العمود الجاف بكثرة في مصابيح الجيب والراديو والأجهزة الإلكترونية الصغيرة.
ب- الخلايا الثانوية
وتسمى أيضا البطاريات السائلة أو الكيميائية كبطارية السيارة) ويتم تصنيعها وفق الآتي:
١- اللوح السالب من مادة الرصاص (Pb).
٢- اللوح الموجب من مادة ثاني أوكسيد الرصاص ( PbO).
٣- تجمع الألواح المالية سوية وتربط بتوصيلة من الرصاص ذات نهاية بارزة تكون القطب السالب ومثلها للقطب الموجب.
٤- توضع المجموعات داخل صندوق أو علبة مصنوعة من مادة عازلة مثل المطاط الصلب الذي يحتوي على حامض الكبريتيك المخفف.
٥. ق.د.ك للعمود الواحد = ٢ فولت
تعتمد فكرة عمل البطارية السائلة (الكيميائية) على قاعدة كيميائية تقول أن: (إذا عمر لوحان موصلان من نوعين مختلفين في حامض كيميائي " ويسمى الالكتروليت"، فإن هذا الحامض سيعمل على فصل الإلكترونات من أحد اللوحين، وترسيب هذه الإلكترونات على اللوح الآخر مما يؤدي إلى الشوء فرق جهد بين اللوحين الموصلين). والشكل (2-2) يوضح شكل البطارية السائلة.
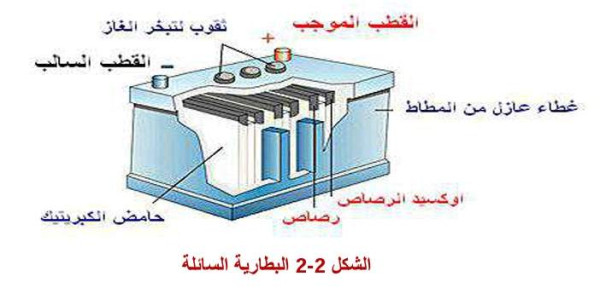
الشكل 2-2 البطارية السائلة
ومن مميزاتها أنه يمكن إعادة شحنها. لقد اتفق على توحيد الفولتيات المستخدمة في البطاريات الذكر منها فولتية البطاريات الجافة مثل (1.5) و (٦) و (۹) فولت وفولتيات البطاريات السائلة مثل (6) فولت (۱۲) فولت و (٢٤) فولت. والشكل (۲-۳) يمثل رمز العمود الكهربائي والبطارية وهي تمثل .(ق.د.ك)
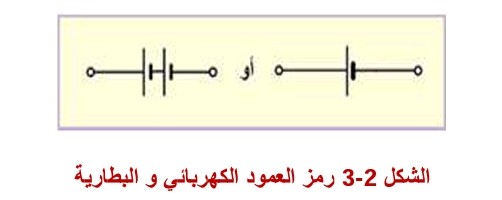
الشكل 2-3 رمز العمود الكهربائي و البطارية
ونظرا لأهمية البطارية القابلة للشحن سنتطرق إلى أنواع مختلفة منها:
١- بطارية الليثيوم بوليمر Lithium-polymer Batteries (Li-poly)
تعد بطارية الليثيوم بوليمر الموضحة في الشكل (2-4) أحدث تقنية للبطاريات المستخدمة في الأجهزة المختلفة وتمتاز بصغر الحجم وخفة الوزن ولها سعة عالية.

الشكل 2-4 بطارية الليثيوم بوليمر
٢. بطارية ايون الليثيوم Lithium Ion Battery (Li-Ion)
تعد هذه البطارية النوع الأكثر شيوعا لبطاريات الهاتف الجوال (الأجهزة الخلوية) إلا أنها تعد غالية الثمن وذات عمر أطول وذات وزن اخف بكثير من مثيلتها من بطاريات النيكل (Nickel Metal) لاحظ الشكل (2-5)، ومن خصائص هذا النوع من البطاريات هو أنها تتلف عند شحنها لأكثر من 24 ساعة

الشكل 2-5 المظهر الخارجي لبطارية ايون الليثيوم
بطارية النيكل-كادميوم Nickel Cadmium (Nied)
وهي بطارية ذات تقنية ليست بالحديثة قابلة للشحن عدة مرات وقد اعتاد عليها الناس لكثرة استخدامها لاحظ الشكل (2-6) أما العناصر الفعالة فيها فهي:
١. المركب (Ni(OH للوح الموجب.
٢. مزيج الكادميوم أو أوكسيد الكادميوم مع الحديد (Iron).
٣.محلول (Electrolyte)
ولهذه البطارية مزايا حسنة منها أن خسائر الدائرة المفتوحة (Open Circuit) لها تكون واطنة جدا أي أنها تفقد شحنها خلال فترة طويلة مقارنة بالأنواع الأخرى. لاحظ الشكل (2-7)

الشكل 2-7 بطارية النيكل - كادميوم مركبة

الشكل 2-6 بطارية النيكل - كادميوم مفردة
بطارية هيدريد معدن النيكل Nickel Metal Hybrid (NiMH)
تفضل هذه البطارية على بطارية النيكل كادميوم لكونها لا تحتوي على الكادميوم وكذلك تصنع من مواد غير سامة (Non-Toxic) وغير ملوثة للبيئة كما أن لها سعة أكبر مقارنة بالأنواع الأخرى من البطاريات ووزنا أخف. إن تقنية بطارية الموبايل الهيدريد معدن النيكل تعد حديثة نسبيا ، لاحظ الشكل (2-8). ولأجل الحصول على أفضل أداء لهذه البطارية ينصح بتفريغها كليا بعد كل عشرين مرة يتم فيها شحنها.

الشكل 2-8 بطارية هيدريد معدن النيكل